肿瘤细胞适应炎性肿瘤微环境(TME)并对免疫疗法产生抗性,其中铁死亡是肿瘤细胞死亡的主要形式。然而,肿瘤细胞通过协调TME刺激及其独特的代谢特征来逃避铁死亡并对免疫疗法产生耐药性的机制仍不清楚。
2025年4月25日,浙江大学许大千、南通大学Tang Zhiyuan、 哈尔滨医科大学Wu Xiaohong共同通讯在Nature Chemical Biology(IF=13)在线发表题为“PSAT1 impairs ferroptosis and reduces immunotherapy efficacy via GPX4 hydroxylation”的研究论文,该研究表明PSAT1通过GPX4羟基化损害铁死亡并降低免疫治疗效果。
在这里,研究人员发现干扰素-γ (IFNγ)激活的钙/钙调素依赖性蛋白激酶II磷酸化丝氨酸337位的磷酸丝氨酸氨基转移酶1(PSAT1)(S337),使其与谷胱甘肽过氧化物酶4 (GPX4)相互作用并稳定蛋白质,对抗铁死亡。PSAT1通过促进α-酮戊二酸依赖的PHD3介导的GPX4脯氨酸159 (P159)羟基化,破坏其与HSC70的结合并抑制自噬介导的降解来提高GPX4的稳定性。在小鼠中,PSAT1 S337A或GPX4 P159A的重建促进了铁死亡并抑制了三阴性乳腺癌(TNBC)进展。在三阴性乳腺癌,用CPP阻断PSAT1 pS337可提高IFNγ诱导的铁死亡并增强程序性细胞死亡蛋白1 (PD-1)抗体的疗效。此外,PSAT1介导的GPX4羟基化与三阴性乳腺癌患者的免疫治疗结果不佳相关,这突出了PSAT1在抑制铁死亡和免疫治疗敏感性方面的非特异性作用。
肿瘤微环境(TME)衍生的细胞因子在塑造肿瘤细胞的代谢景观中起着重要作用。代谢重编程是癌症的标志之一,有助于肿瘤免疫和代谢的异质性,这极大地影响了肿瘤细胞的死亡逃避和当前的治疗脆弱性。免疫检查点阻断(ICB)疗法通过增强T细胞介导的肿瘤清除,彻底改变了癌症治疗。遗憾的是,由于频繁的进展事件,客观缓解率仍然远远不能令人满意,因为只有大约10-30%的患者可以从作为单一药物的治疗中受益。然而,肿瘤对ICB疗法反应的代谢决定因素仍然知之甚少。
肿瘤细胞表现出频繁的代谢重新编程,揭示了其代谢途径中独特的脆弱性,可以通过诱导特定形式的代谢细胞死亡来进行治疗。铁死亡,一种由脂质驱动的铁依赖性细胞死亡途径的过氧化作用是癌症治疗中的一个关键弱点。谷胱甘肽(GSH)依赖性磷脂氢过氧化物酶GSH过氧化物酶4 (GPX4)是一种重要的硒酶,可将细胞毒性脂质氢过氧化物转化为无细胞毒性的脂质醇,在预防铁死亡中具有重要作用。涉及GPX4抑制的策略已越来越多地用于诱导癌细胞死亡,单独使用或与其他疗法(如ICB疗法)联合使用。氨基酸转运蛋白溶质载体家族7成员11 (SLC7A11)促进胱氨酸摄取,导致增强GPX4蛋白合成和代谢酶的非代谢功能,如肌酸激酶B,其影响GPX4稳定性并抑制胰岛素样生长因子1 (IGF1)治疗下的铁死亡。然而,在特定的TME(如干扰素-γ (IFNγ)刺激)中,关键的铁死亡调节因子GPX4是如何被操纵的,以及这种调节对肿瘤细胞逃避铁死亡的影响(这可能导致不利的免疫治疗反应)仍然难以捉摸。
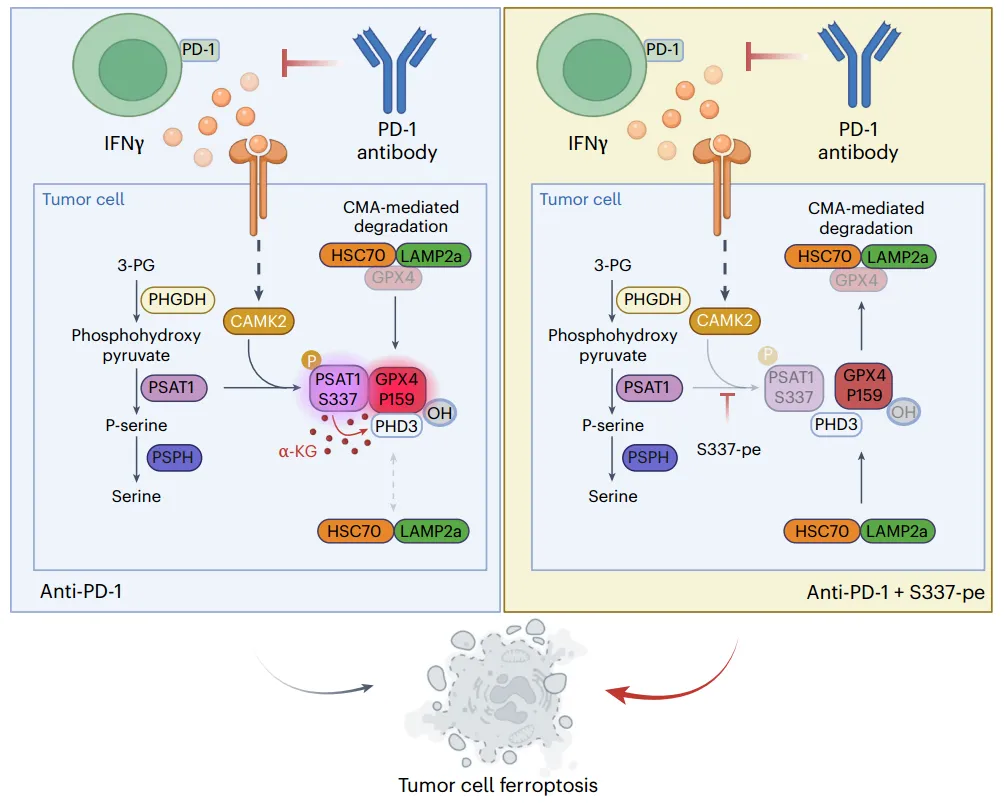
PSAT1产生的α-KG促进PHD3介导的GPX4羟基化以抑制铁死亡
(图源自Nature Chemical Biology)
在肿瘤发展过程中,代谢酶及其副产物的活性或功能失调的驱动下,代谢重编程与多种细胞过程密切相关。丝氨酸代谢在多种类型的癌症中被上调,通过为大分子合成提供构件或与单碳代谢偶联以保持氧化还原平衡来支持肿瘤增殖和转移。磷酸丝氨酸氨基转移酶1 (PSAT1)是丝氨酸合成途径中的关键酶,催化3-磷酸羟基丙酮酸和谷氨酸转化为3-磷酸丝氨酸和α-酮戊二酸(α-KG)。PSAT1的上调出现在各种癌症中,并促进细胞增殖、转移和治疗抗性。然而,肿瘤细胞特异性丝氨酸代谢重编程和肿瘤铁死亡脆弱性之间复杂的相互调节作用尚未完全了解。此外,目前尚不清楚PSAT1是否能在特定的TMEs中发挥非冠状功能(如IFNγ刺激),这可能会潜在地损害ICB治疗的有效性。
该研究证明PSAT1的非经典功能促进了GPX4的表达。TME衍生的IFNγ激活的钙/钙调素依赖性蛋白激酶II (CAMK2)在丝氨酸337磷酸化PS AT1(S337),这增加了PS AT1-GPX4的相互作用。GPX4相关的PSAT1产生α-KG,促进PHD3介导的GPX4羟基化。这种级联反应增强了GPX4的稳定性,并有效抑制了影响ICB治疗效果的铁死亡。此外,还开发了一种细胞穿透肽(CPP ),抑制PSAT1上S337的磷酸化,这为提高肿瘤对铁死亡的敏感性和改善ICB疗法的反应性的策略提供了线索。总之,该研究发现阐明了PSAT1在铁死亡调节中的非经典功能,并揭示了PSAT1是癌症治疗的一个有吸引力的靶点。
参考信息:https://www.nature.com/articles/s41589-025-01887-3#Sec41
