血小板稳态在维持血管完整性和免疫防御中至关重要。尽管血小板的形成过程已经得到广泛研究,但巨核细胞(MKs)生成的细胞机制和分子机制仍不清楚,其中涉及到巨核祖细胞(MKPs)生成,用以不断补充MKs的过程。
近日,来自德国慕尼黑大学附属医院的Florian Gaertner团队在Nature期刊发表题为Plasmacytoid dendritic cells control homeostasis of megakaryopoiesis(浆细胞样树突状细胞调控巨核细胞生成稳态)的文章。研究人员揭示了浆细胞样树突状细胞(pDCs)通过监测骨髓中的凋亡MKs并释放IFNα,促进局部MK祖细胞的增殖和成熟,维持血小板和MKs生成在稳态和应激状态下的平衡。
血小板是血液循环中的无核细胞,对于维护血管屏障功能至关重要。它们由其前体细胞——MKs在骨髓中生成,这个过程被称为血小板生成(thrombopoiesis)。在血小板生成期间,MKs会表现出凋亡迹象,并在其细胞破碎过程中释放出血小板。因此,为了确保MKs的稳态以及血小板的持续形成,必须通过MKs生成作用不断补充消耗的MKs,这一过程依赖于MKs祖细胞的增殖和分化。
MKs的生成
首先,研究人员探讨了骨髓中MKs的生成及其与血小板生成的关系。研究发现,成熟的MKs主要分布在骨髓窦道附近,其形成过程涉及从MKPs向MKs的转变。成熟MKs在血小板生成完成后迅速减小和消失,同时在其周围产生新的MKPs,用于产生成熟的MKs,维持血小板生成的稳态。在血小板需求增加时,MKPs快速增殖以迅速补充血小板,保持循环血小板的平衡。这些发现揭示了骨髓中MKs生成和血小板生成过程之间密切的协调机制,无论在正常或病理状态下,都能确保血小板生产的有效性和MKs的稳定性。
IFNα驱动pDC对MK生成的调控
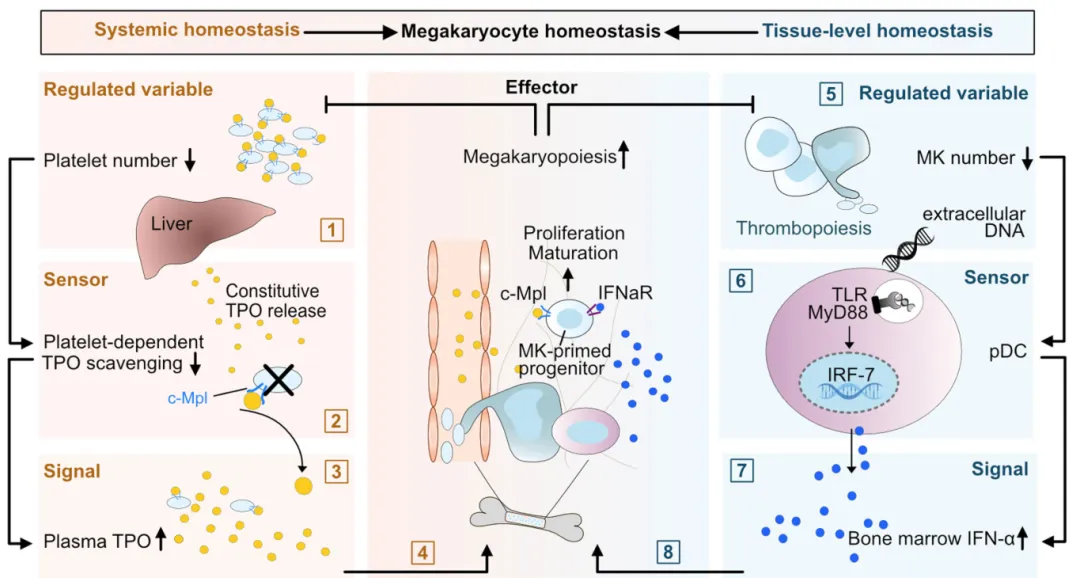
肝源性血小板生成素(TPO)是促进MKs生成的有效细胞因子,其血浆水平受到循环血小板表面TPO 受体(cMPL)的严格调控。尽管升高的TPO能够促进骨髓中MKPs的增殖,但并未直接引发血小板缺失(PD)后局部血管周围典型的MKs生成。研究显示,即使在TPO和cMPL缺失的小鼠中,仍能在应激条件下将血小板数量恢复到正常,暗示可能存在与TPO无关的其他信号调控机制。研究还表明,成熟MKs显示出凋亡迹象,尤其是在血小板消耗引发的急性MKs生成时,凋亡现象更加显著。这表明凋亡MK可能在血管周围微环境中触发局部MKPs的自我替换。此外,研究还发现,虽然巨噬细胞在稳态中与MKs接触,但其消耗并未显著改变MKs生成或血小板生成。因此,巨噬细胞在这一过程中的贡献相对较小,提示其他吞噬细胞亚群可能在调控凋亡MKs清除和MKs生成中扮演重要角色。pDCs是一种特殊的固有免疫细胞亚群,专门检测凋亡细胞和核酸,在骨髓中丰度较高。研究人员使用BDCA2-DTR小鼠模型和抗体清除方法,发现pDCs的去除显著减少了骨髓中的MKs和MKPs数量,导致外周血小板数量下降。这些结果不仅揭示了pDCs在维持血小板生成中的关键作用,还显示了它们在MKs生成微环境中的调节作用。特别是在应激状态下,pDCs的去除可以完全消除血小板减少所引起的急性MKs生成,表明pDCs能够刺激MKs生成,并确保稳态和应激条件下维持MKs和血小板数量的稳定。进一步的研究显示,pDCs遇到凋亡细胞时,通过IRF7依赖的方式被激活,并释放IFNα到微环境中,维持骨髓中的IFNα水平。随着血小板需求的增加,MKs的凋亡数量增加,从而可以增强活化pDCs的作用。随后,pDCs可以感知MKs来源的细胞外DNA,通过MYD88-IRF7信号通路产生I型干扰素,参与MKs稳态的维持。研究还发现,pDCs通过释放IFNα调控骨髓细胞外液中的IFNα水平,这对于维持MKPs的扩增和成熟至关重要。在应激情况下,如血小板减少时,pDCs释放的IFNα能够迅速促进MKs生成,通过增加MKs数量和MKPs的发育,最终促进血小板的增加。单细胞转录组分析显示,pDCs依赖的MK前体细胞表达与细胞分裂、翻译和干扰素响应相关的基因,特别是在循环巨核细胞-红细胞祖细胞前体(MK-MEPs)中表达水平最高。实验还证实,pDCs的缺失或IFNα信号通路中断均导致MKs生成受阻,进一步证明IFNα是pDCs调控MKs生成的主要介导因子。总的来说,pDCs通过将IFNα释放到骨髓微环境,进而通过IFNAR信号促进MK祖细胞的扩增和成熟,维持稳态和应激下的血小板生成。这些研究揭示了pDCs在调节MKs生成和血小板稳态中的重要作用,为深入理解血小板生成的分子机制提供了新的视角。
pDC-MK接触与人类疾病有关
研究人员对人类骨髓样本中pDC-MK的作用进行了深入探讨,发现在稳态和血小板减少时,pDCs通过增加MKs数量和发育显著促进血小板的生成。在健康人群和重型免疫性血小板减少性紫癜(ITP)患者中,pDC与MK的接触显著增加,这表明pDCs在人类骨髓中的MKs周转中起着重要的调控作用。由于pDCs是抗病毒免疫中IFNα的主要来源,研究人员假设,在急性感染情况下,病毒可以激活pDCs并释放大量IFNα,超过MKs所需的稳态范围,导致异常的MKs增生,这在与病毒感染相关的疾病如COVID-19中尤为显著。分析还显示,COVID-19患者和SARS-CoV-2感染的小鼠骨髓中pDCs数量显著增加,并且pDCs与MK的接触增加了三倍,这与观察到的MKs增生密切相关。进一步实验表明,通过阻断IFNα信号传导,可以减少pDC与MK的接触,并避免COVID-19中MKs异常增生的发生。这些结果表明,严重的系统性感染可能干扰pDCs对MKs生成的正常调控,从而导致MKs的异常变化。
综上所述,该研究发现pDCs通过识别凋亡MKs释放的DNA,激活MYD88-IRF7信号通路并释放IFNα,从而促进MKs生成,维持血小板平衡。如果pDCs功能出现紊乱,可能导致MKs的异常增生,进而引发炎症和血小板数量的变化。这些发现为感染性疾病的治疗提供了新的视角。
原文链接:https://doi.org/10.1038/s41586-024-07671-y
