以奥希替尼为代表的第三代EGFR酪氨酸激酶抑制剂(TKIs)在治疗非小细胞肺癌(NSCLC)方面显示出良好的临床疗效。之前的工作已经确定ASK120067是一种新型的第三代EGFR TKI,具有显著的抗肿瘤效果,已在中国进行了新药上市申请(NDA)的提交。尽管取得了实质性进展,但对EGFR-TKIs的获得性耐药仍然是一个重大挑战,阻碍了治疗方法的长期有效性。
2024年8月15日,中国科学院大学谢华、周虎、丁健、赵桂龙共同通讯在Signal Transduction and Targeted Therapy在线发表题为”Branched-chain amino acid transaminase 1 confers EGFR-TKI resistance through epigenetic glycolytic activation“的研究论文,该研究利用高通量蛋白质组学分析对已建立的TKI耐药肿瘤模型进行了全面研究,发现与亲本TKI敏感的NSCLC肿瘤相比,奥希替尼和ASK120067耐药肿瘤中的支链氨基酸转氨酶 (BCAT1)表达显著上调。
BCAT1 的基因耗竭或药理抑制损害了耐药细胞的生长,并使肿瘤细胞对 EGFR TKI 部分重新敏感。机制上,抗性细胞中上调BCAT1重编程了支链氨基酸 (BCAA)代谢,促进了赖氨酸27在组蛋白H3(H3K27)上的α-酮戊二酸(α-KG)依赖性去甲基化以及随后的糖酵解相关基因的转录去抑制,从而增强了糖酵解并促进肿瘤进展。此外,研究发现WQQ-345是一种新型BCAT1抑制剂,在体外和体内均对TKI耐药肺癌具有抗肿瘤活性,BCAT1高表达。综上所述,该研究强调了BCAT1在通过表观遗传激活糖酵解介导对第三代EGFR-TKIs的耐药性方面的关键作用,从而支持BCAT1作为治疗TKI耐药NSCLC的有前途的治疗靶点。
对表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)的耐药被认为是EGFR突变非小细胞肺癌(NSCLC)患者治疗失败和癌症复发的主要原因。奥希替尼(AZD9291)是被广泛批准用于EGFR T790M突变NSCLC标准二线治疗和EGFR激活突变NSCLC一线治疗的代表性化合物。此外,ASK120067是一种新型的第三代EGFR TKI,研究团队报道了具有良好抗肿瘤疗效的药物,目前正在中国进行新药上市申请(NDA)。尽管第三代EGFR TKIs具有显著的临床前和临床疗效,但获得性耐药性不可避免地会出现。然而,超过30%的奥希替尼耐药机制仍未得到解释,这吸引了对新的耐药机制和潜在治疗策略的探索,以治疗TKI耐药的NSCLC。
代谢重编程被认为是恶性肿瘤的主要标志之一,对基因组稳定性、细胞增殖和肿瘤微环境有着深远的影响。氨基酸为蛋白质合成提供基石,并作为增殖细胞所需的能量和代谢物来源。支链氨基酸(BCAA)是必需氨基酸,不仅可以作为营养底物,而且还可以降解为参与肿瘤发生的其他途径提供多种代谢物。在细胞中,支链氨基酸转氨酶(BCATs),通过将氨基从 BCAA 转移到α-酮戊二酸(α-KG)以产生谷氨酸及其相应的支链酮酸(BCKA)来启动BCAA代谢。随后,BCKAs通过线粒体中的支链α-酮酸脱氢酶(BCKDH)复合物进行脱羧,最终代谢为乙酰辅酶A和琥珀酰辅酶A,以促进三羧酸(TCA)循环。在许多类型的人类癌症中,BCAA代谢改变与肿瘤进展有关。虽然一些研究展示了BCAA代谢在NSCLC中的潜在致癌作用,但肿瘤细胞如何协调致癌BCAA代谢以支持NSCLC的进展仍然在很大程度上难以捉摸。此外,尚未报道针对 BCAA 代谢的药物用于 NSCLC 治疗。
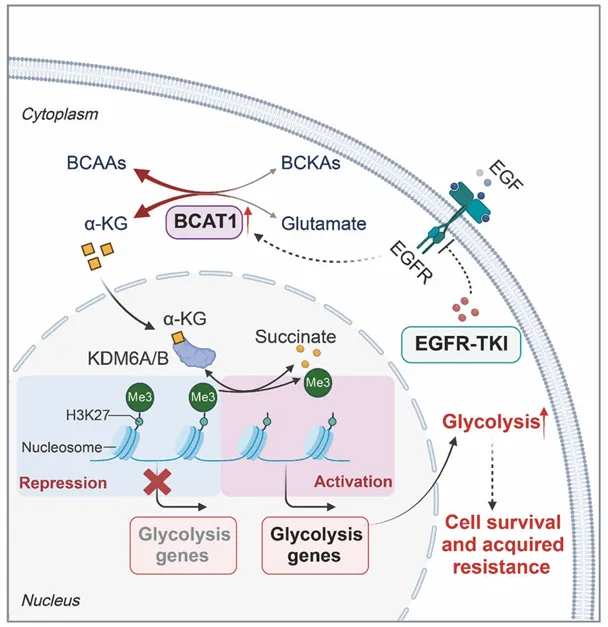
BCAT1介导的EGFR-TKI通过α-KG依赖性糖酵解表观遗传激活的抵抗性示意图(图源自Signal Transduction and Targeted Therapy)
α-KG在多种生物过程中起着关键作用。作为 2-氧代戊二酸(2-OG)依赖性双加氧酶的底物,α-KG刺激羟化酶,如脯氨酰羟化酶(PHDs)和抑制因子 HIF-1α 1(FIH-1)以限制 HIF-1α 信号传导的活性。此外,α-KG通过激活Jumonji-C (JmjC)家族赖氨酸去甲基化酶(kdm) (JmjC- kdm)和10 - 11易位(TET)酶(分别介导组蛋白和DNA去甲基化)来影响基因表达和细胞干性。此外,谷氨酸脱氢酶1(GLUD1)介导的α-KG产生有助于触发多西他赛或吉非替尼耐药肺癌的上皮-间充质转化。尽管如此,将α-KG与耐药性联系起来的确切机制仍不清楚。
在这项研究中,作者采用高通量蛋白质组学分析来表征获得性抗性时蛋白质组的改变,旨在确定对第三代EGFR TKIs的新耐药机制。与TKI敏感细胞相比,BCAT1在TKI耐药细胞中是一种高度上调的蛋白质,在体外和体内支持细胞存活和维持耐药性方面起着关键作用。从机制上讲,BCAT1 的过表达加速了BCAA合成代谢,以促进TKI抗性细胞中糖酵解基因的α-KG 依赖性表观遗传学激活,从而增强糖酵解以维持细胞活力并介导耐药性。此外,该研究开发并表征了WQQ-345作为一种新型的BCAT1靶向抑制剂,并证明了其对TKI耐药NSCLC肿瘤的体外和体内抗肿瘤功效。
参考消息:https://www.nature.com/articles/s41392-024-01928-8
