进食节律调节运动表现和肌肉能量代谢。然而,调节脂肪细胞功能的机制仍不清楚。
2025年3月14日,陆军军医大学李旻典、张志辉共同通讯在Cell Metabolism(IF=27.7)在线发表题为“Dietary timing enhances exercise by modulating fat-muscle crosstalk via adipocyte AMPKα2 signaling”的研究论文,该研究表明定时饮食通过脂肪细胞AMPKα2信号调节脂肪-肌肉串扰增强运动。
该研究使用多组学分析,包括(磷酸)蛋白质组学和脂质组学,发现日间限时饮食(DRF)调节小鼠性腺白色脂肪组织(GWAT)中线粒体蛋白质组、中性脂质组和营养感应途径的昼夜节律。脂肪细胞特异性敲除AMPKα2(编码AMPKα2的基因)会削弱身体耐力。这种缺陷与酰基辅酶A (CoA)代谢相关基因的节律性改变、GWAT脂质团节律性丧失和血清代谢物(特别是乳酸和琥珀酸)的昼夜节律重塑有关。我们还发现脂肪细胞Prkaa2在DRF期间调节肌肉时钟基因。值得注意的是,口服AMPK激活剂C29以一天中的时间方式增加耐力和肌肉功能,这需要完整的脂肪细胞AMPKα2信号。总的来说,该研究将脂肪细胞AMPKα2信号定义为脂肪和肌肉之间昼夜代谢协调的关键调节因子,从而提高运动表现。
身体耐力需要不同器官系统的协调行动。工作肌肉分泌信号代谢物,包括琥珀酸、细胞外囊泡,激素和细胞因子,以增加线粒体代谢和脂解,赋予心脏代谢健康。在有氧运动期间,肌肉组织能够实现从糖酵解到氧化磷酸化和脂肪氧化的代谢转换,而脂肪组织动员脂肪并释放脂肪因子或脂因子以应对代谢需求。其他组织在运动期间或之后通过激素和神经信号调节肌肉代谢。新出现的证据将昼夜节律与运动代谢联系起来。例如,一次跑步机跑步会引起七种组织代谢物昼夜节律的时间依赖性反应。
能量保存和身体耐力受进食节律的不同调节。小鼠在活跃期进食,或夜间限制进食(NRF,类似于人类的16:8禁食),可加强能量代谢的昼夜节律,并在西方饮食喂养方案中预防肥胖、脂肪肝和糖尿病。这仅与雄性在抗阻运动中的表现改善有关。NRF部分通过改善宏量营养素利用和增加脂肪细胞产热来激活能量代谢。肝脏NADH循环通过Sirt1的节律性表达将产热和摄食节律联系起来。相比之下,白天限制进食(DRF或反相进食,类似于人类的斋月式禁食)与常规食物饮食相结合,增加了雄性和雌性久坐小鼠以及受过训练的小鼠的肌肉氧化能力和耐力。肌肉和肝脏组织中由Per2、Rev-erbα和Hdac3介导的昼夜节律钟改变了运动耐力的昼夜差异。有趣的是,DRF在整个光暗周期中持续增加耐力。
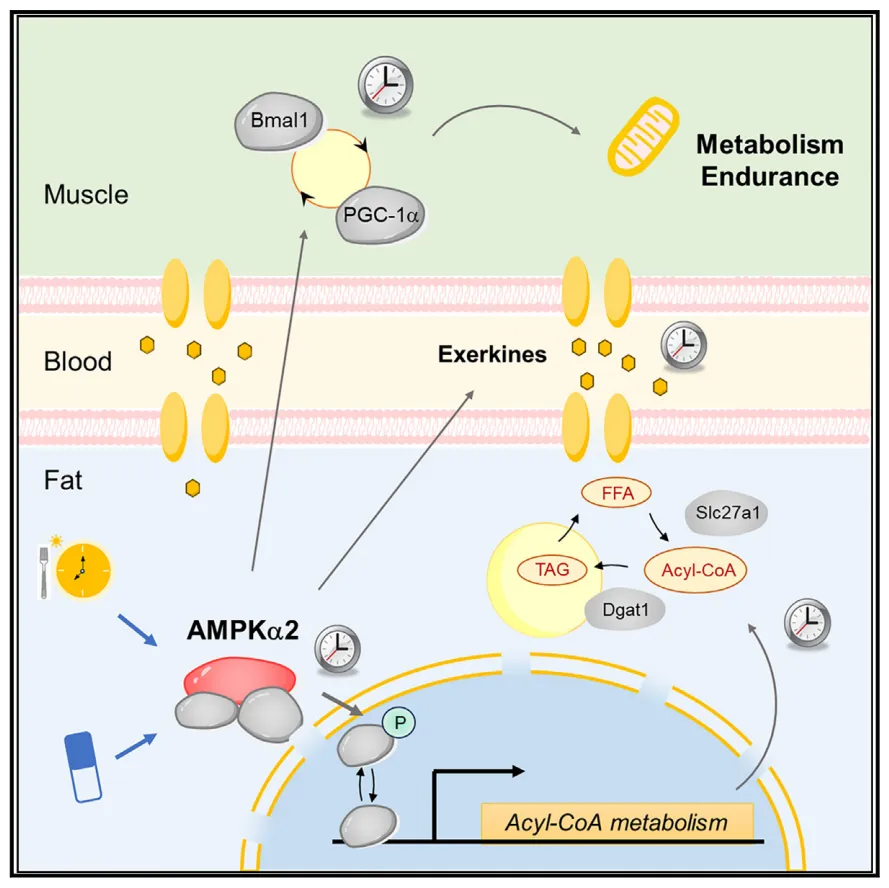
机理模式图(图源自Cell Metabolism )
在这里,研究人员采用了一种系统方法,通过最先进的定量蛋白质组学、脂质组学和磷酸蛋白质组学在DRF/NRF小鼠的GWAT中描绘节律蛋白。该系统分析确定脂肪细胞线粒体代谢和腺苷酸活化蛋白激酶(AMPK) α2信号通路是与DRF相关的关键昼夜信号。该研究证明了脂肪细胞AMPKα2信号的昼夜节律计时通过喂食时间表或AMPK激活剂增加了跑步耐力,这需要脂肪AMPKα2在生物黎明时的活性,并且与小鼠中脂肪到肌肉的昼夜串扰相关。根据AMPKα2信号传导的DRF相关多组学特征,脂肪细胞AMPK激活剂对AMPKα2信号传导途径的昼夜节律性激活增强了小鼠的跑步耐力,这可能使时间医学方法能够改善体能。
原文链接:https://www.cell.com/cell-metabolism/fulltext/S1550-4131(25)00065-8
