SEL1L介导的内质网相关降解(ERAD)通过降解错误折叠或末端未折叠的蛋白质在控制蛋白质稳态中起关键作用。然而,SEL1L如何调节外周T细胞存活和体内平衡尚不清楚。
2023年8月30日,中国医学科学院系统医学研究院/苏州系统医学研究所张连军、西安交通大学张保军及苏州大学张进平共同通讯在Cellular & Molecular Immunology(IF=24)在线发表题为“SEL1L preserves CD8+ T-cell survival and homeostasis by fine-tuning PERK signaling and the IL-15 receptor-mediated mTORC1 axis”的研究论文,该研究发现SEL1L缺失导致成熟T细胞的频率和数量大大减少,同时还会诱导多种形式的细胞死亡。此外,SEL1L缺陷选择性地破坏了naïve CD8+ T细胞的稳态,正如naïve T细胞亚群的严重丢失而记忆T细胞亚群的增加所表明的那样。作者还发现,SEL1L缺失促进了mTORC1/c-MYC的激活,并诱导了代谢转移,这主要是由于IL-15受体α和β链的表达增强。
从机制上看,单细胞转录组分析和生化分析进一步揭示,Sel1l−/−CD8+ T细胞存在过度的内质网应激,特别是PERK-ATF4-CHOP-Bim通路的异常激活,通过补充IL-7或IL-15可以缓解。重要的是,PERK抑制极大地解决了Sel1l−/−CD8+ T细胞的存活缺陷。此外,IRE1α缺乏通过下调IL-15受体α链降低Sel1l−/−naïve CD8+ T细胞中的mTORC1信号通路。总之,这些观察结果表明,ERAD接头分子SEL1L通过调节PERK信号级联和IL-15受体介导的mTORC1轴,作为一个重要的检查点,保护外周T细胞的生存和稳态。
严格的蛋白质平衡系统确保了细胞内蛋白质组的平衡和功能的微妙调节。内质网中错误折叠或聚集的蛋白质通过内质网相关降解(ERAD)途径被选择性地识别和降解。哺乳动物细胞已经进化出非常复杂的ERAD系统,越来越多的证据表明,至少有10个ERAD分支具有各自的泛素连接酶和底物。含有Lin-12-like (SEL1L)和HRD1抑制/增强子的复合物是真核生物中最保守的ERAD分支,含有大量底物。SEL1L是维持HRD1稳定性和招募底物的重要接头分子。已有研究表明,SEL1L/HRD1 ERAD复合物在调节食物摄取、水分平衡、全身能量稳态和脂质代谢等方面具有不可或缺的生理意义。值得注意的是,棕色脂肪细胞中SEL1L的缺失导致巨型线粒体的形成,巨型线粒体在形态上扩大,形状异常。
因此,由于ER-线粒体接触和线粒体动力学失调,线粒体功能严重受损。此外,造血干细胞(HSCs)中SEL1L的缺失会导致过度增殖,并损害长期的自我更新潜能。此外,SEL1L已被证明通过限制mTOR活性和MPL (HSC身份的主要调节因子)来保持HSC的静止和自我更新能力。同样,最近的一项研究表明,SEL1L作为一个关键的蛋白质质量控制检查点,控制胸腺β选择和DN3到DN4的转换。有趣的是,该研究表明,Notch细胞内结构域对于ERAD核心基因(包括SEL1L和HRD1)的转录至关重要。
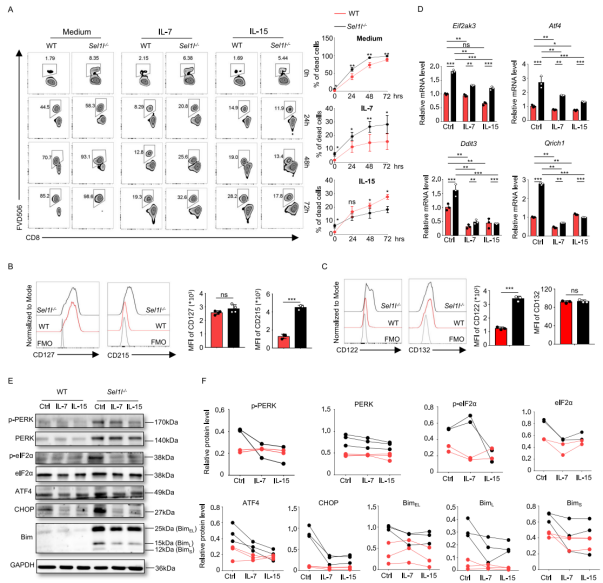
IL-7和IL-15通过抑制PERK/ATF4/CHOP/Bim信号通路来挽救Sel1l−/−CD8+ T细胞的存活(图源自Cellular & Molecular Immunology )
Naïve T细胞稳态是通过强直性T细胞受体信号传导和细胞因子刺激来维持的。鉴于SEL1L在调节HSC静止和胸腺细胞发育中的关键作用,该研究旨在研究SEL1L介导的ERAD通路是否以及如何在稳态条件下调节外周血naïve T细胞稳态。在此,通过使用T细胞特异性SEL1L敲除小鼠模型,作者证明SEL1L缺陷导致胸腺和外周成熟T细胞数量显著减少。在过继性骨髓移植和竞争性骨髓移植实验中,Sel1l−/− T细胞在很大程度上被WT T细胞打败。重要的是,在SEL1L缺失的情况下,naïve CD8+而不是CD4+ T细胞的维持被严重破坏,正如CD62L+CD44- naïve T细胞群的显著缺失和CD62L+CD44+和CD62L- CD44+ T细胞群的增加所表明的那样。
从机制上讲,SEL1L缺陷导致PERK-ATF4 -CHOP-Bim过度激活,而抑制PERK在很大程度上挽救了SEL1L−/−CD8+ T细胞的存活。此外,SEL1L缺陷通过降低表面TCRβ和CD3的表达,选择性地损害了成熟CD8+而不是CD4+ T细胞的补充性TCR信号。此外,SEL1L缺陷导致IL-15受体表达和信号传导升高,从而增强mTORC1/c-MYC的激活。相反,IRE1α缺失通过减少IL-15受体α链减弱Sel1l−/−naïve CD8+ T细胞中的mTORC1信号。综上所述,这些发现为了解SEL1L介导的ERAD通路在保护成熟CD8+ T细胞的存活和稳态中的作用提供了重要的见解。
原文链接:https://www.nature.com/articles/s41423-023-01078-x
