近日,圣路易斯华盛顿大学的一支研究团队在权威期刊Neuron上发表论文,为治疗阿尔茨海默病提出了一种有潜力的方法:给脑细胞“降脂”。模拟阿尔茨海默病的动物模型显示,利用实验药物清除脑细胞中积累的胆固醇,可减少神经退行性变,防止脑损伤。

其实,脂质代谢与阿尔茨海默的关系早已受到研究者的关注。这是因为,被公认为迟发型阿尔茨海默病的最强遗传风险因素APOE4,编码的就是一种与脂质代谢有关的蛋白质,即载脂蛋白E(ApoE)。顾名思义,这种蛋白在血液中携带胆固醇等脂质分子。
而在脑组织中,APOE基因涉及胆固醇平衡和运送有关的信号通路,会影响神经元、小胶质细胞、星形胶质细胞等多种脑细胞的脂质代谢。先前的一些研究表明,携带APOE4的细胞在胞体内堆积了异常多的胆固醇。
为了进一步确认APOE、脑细胞脂质代谢和脑损伤之间的关系,在这项研究中,科学家们把人类的APOE4基因转入小鼠体内,替代小鼠原本的APOE基因;与此同时,一部分小鼠转入APOE基因的另一种变异体APOE3作为对照,它不影响阿尔茨海默病风险。
这些实验小鼠还有一个特点:在特定基因的作用下,它们的脑组织内容易积累tau蛋白,而蛋白积累处的神经细胞会退化和死亡,与阿尔茨海默病患者的病理特点很相似。
根据研究人员的观察,这些小鼠从6个月大左右开始出现神经退行性病变的迹象;到9.5个月大时,大脑已经严重受损,像筑巢之类的日常行为已经无法顺利完成。而携带了APOE4的小鼠,其萎缩受损的脑区中可以看到以不寻常的方式聚积了过量胆固醇。脂质组学分析显示,多达180种脂质的浓度发生了改变。
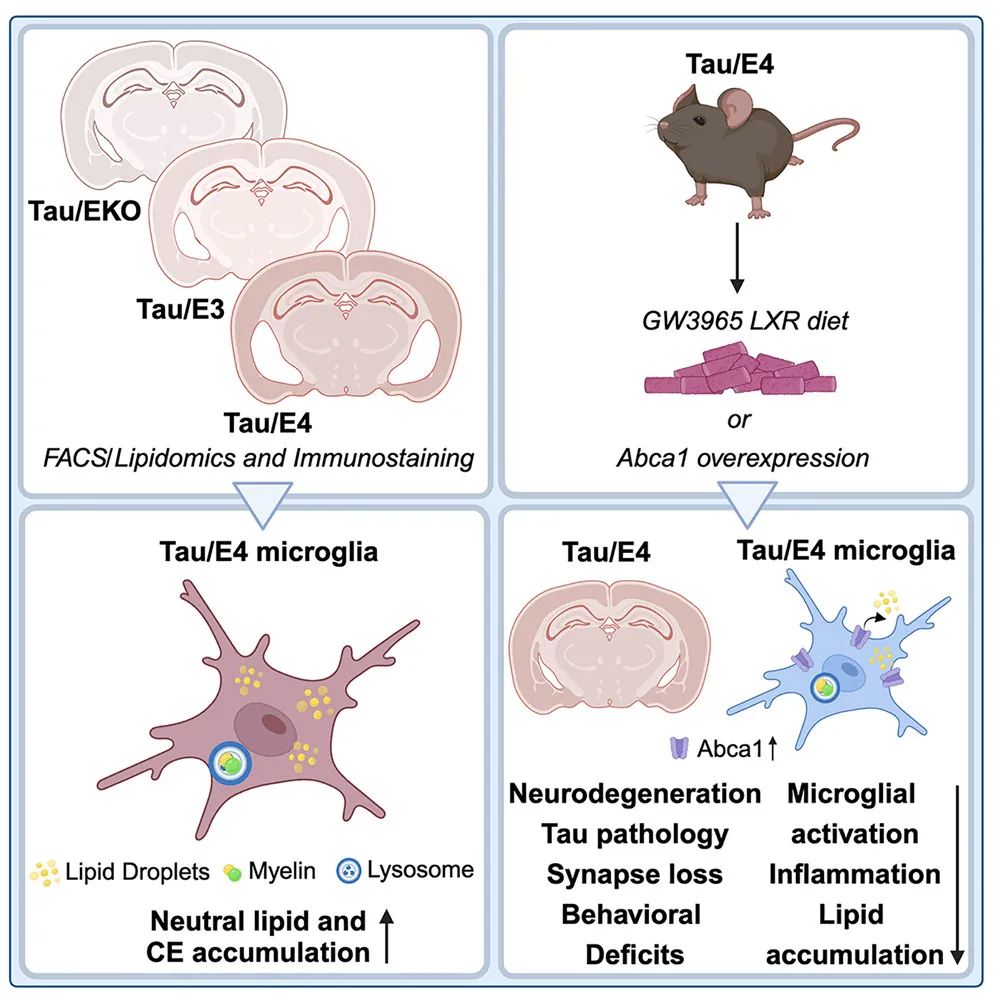
▲研究示意图:携带ApoE4的Tau病理小鼠大脑中,小胶质细胞中脂质堆积过量(右图)(图片来源:参考资料[2]
其中与APOE3小鼠最为显著的差别是,APOE4小鼠的小胶质细胞中堆积了许多胆固醇酯(cholesteryl esters)。这些细胞是大脑的免疫细胞,本应起到保护大脑的作用,但如果在不该被激活的时候激活,则会损害脑组织。而现在,研究人员发现,充满脂质的小胶质细胞就变得过于“激动”,开始分泌炎性因子,对周围组织造成破坏。
于是,接下来研究人员采用了一种实验性药物,帮助这些实验小鼠降低细胞中的脂质水平。这种药物属于肝X受体(LXR)小分子激动剂,通过上调一种名为Abca1的基因,促进细胞排出胆固醇。
小鼠从6个月大时开始服用药物,等到9.5个月大,与服用安慰剂的同伴相比,可以看到它们的脑损伤明显要小得多:包括脑容量获得了更多保留,tau蛋白积累较少,小胶质细胞引起的炎症状况减轻,神经细胞之间的连接受到的损失也更少。从行为表现来看,服用药物的小鼠还保留了一定的筑巢能力。
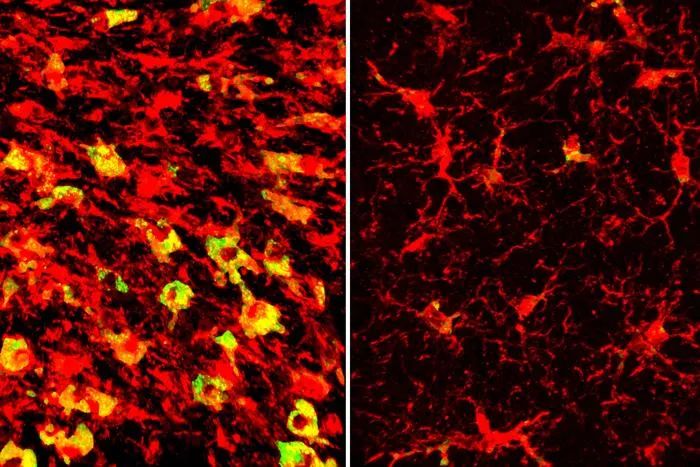
▲模拟AD病理发展的小鼠在用药后,小胶质细胞内的脂质沉积(绿色所示)消失(右图)(图片来源:参考资料[2];Credit:Alexandra Litvinchuk/Washington University)
研究人员在论文中总结说,这些数据提示,促进胶质细胞脂质外流可以作为一种治疗策略,减轻与tau蛋白和ApoE4有关的神经退行性病变。不过研究人员补充说,实验中用到的LXR激动剂目前还有一个亟待优化的地方,那就是它也会影响肝脏中的脂质代谢。为避免引起脂肪肝,药物化学家正在努力设计没有这种副作用的LXR激动剂。一旦成功,新的药物有望对心血管疾病和神经退行性疾病都带来帮助。
参考资料:
[1] Alexandra Litvinchuk et al, Amelioration of Tau and ApoE4-linked glial lipid accumulation and neurodegeneration with an LXR agonist, Neuron (2023). DOI: 10.1016/j.neuron.2023.10.023.
[2] Lowering a form of brain cholesterol reduces Alzheimer’s-like damage in mice. Retrieved Nov. 24, 2023 from https://www.eurekalert.org/news-releases/1008647
