多粘菌素是对抗许多危及生命、耐多药革兰氏阴性菌感染的有效方法,但与多粘菌素相关的细胞毒性和耐药性极大地阻碍了其临床转化。
2024年7月18日,中国科学院大学/南开大学/温州医科大学刘勇、温州医科大学李圆凤、四川农业大学赵兴洪、中国科学院大学Piao Yinzi共同通讯在Advanced Materials 在线发表题为“Reaction-Induced Self-Assembly of Polymyxin Mitigates Cytotoxicity and Reverses Drug Resistance”的研究论文,该研究报道了多粘菌素和天然醛类在水溶液中的反应诱导自组装(RISA),由此产生的组装体有效地掩盖了多粘菌素的正电荷,降低其细胞毒性。
此外,具有代表性的PMBA4(多粘菌素B(PMB)和(E)-2-庚烯醛(A4))组装体与革兰氏阴性细菌外膜的结合显著增强,并表现出多种抗菌机制,包括增加膜通透性、提高细菌代谢、抑制群体感应、减少ATP合成以及降低细菌耐药性。值得注意的是,PMBA4组装体可逆转临床分离的革兰氏阴性菌耐药菌株的耐药性,在预防和根除细菌生物膜方面表现出卓越功效。PMBA4组装体可有效根除体内革兰氏阴性菌生物膜感染并减轻炎症反应。该研究提供了一种实用且临床适用的方法,可最大限度地减少副作用、逆转耐药性并防止出现与游离多粘菌素相关的耐药性。
20世纪40年代,研究人员在土壤样本中发现多粘菌素。他们从多粘芽孢杆菌菌株中分离并鉴定了这些抗生素,由此产生了“多粘菌素”的名称。多粘菌素通过结合革兰氏阴性菌外膜中的脂多糖(LPS)发挥其抗菌活性,产生一些晶体结构破坏膜完整性破坏并增加渗透性,促进细胞内成分和离子的泄漏,最终导致细菌死亡。多粘菌素因对多药耐药肺炎克雷伯菌、鲍曼不动杆菌、铜绿假单胞菌和肠杆菌属等革兰氏阴性菌的有效性而受到关注,在20世纪50年代被引入临床,此后被列为最后手段的抗生素。尽管多粘菌素具有杀菌功效,但可引起肾毒性和神经毒性,导致肾损害和神经相关副作用。此外,细菌对多粘菌素的耐药性已成为一个重大问题,限制了其治疗感染的有效性。最后,多粘菌素所需的静脉给药途径不便,需要专业医疗人员的帮助。因此,迫切需要一种有效的策略来减轻多粘菌素的细胞毒性并逆转其耐药性。
为此,首先需要深入了解多粘菌素的化学结构。临床使用的多粘菌素B(PMB)和E是环状多肽抗生素,因带有碱性氨基酸残基具有阳离子电荷,脂肪酸尾部使其亲脂性增强,有助于稳定的环状排列。目前克服多粘菌素细胞毒性的策略包括结构修饰以降低毒性,同时保持抗菌活性,以及利用纳米级或靶向递送系统来提高选择性并最大限度地减少对哺乳动物细胞的影响。多粘菌素的化学结构修饰可能导致药代动力学改变、抗菌活性丧失、复杂性和成本增加、脱靶效应和免疫检测变化,而纳米载体负载多粘菌素的主要驱动力是带正电荷的多粘菌素分子与带负电荷的纳米载体表面之间的静电相互作用。然而,此类负载方法存在药物负载能力有限、过早释放等问题。
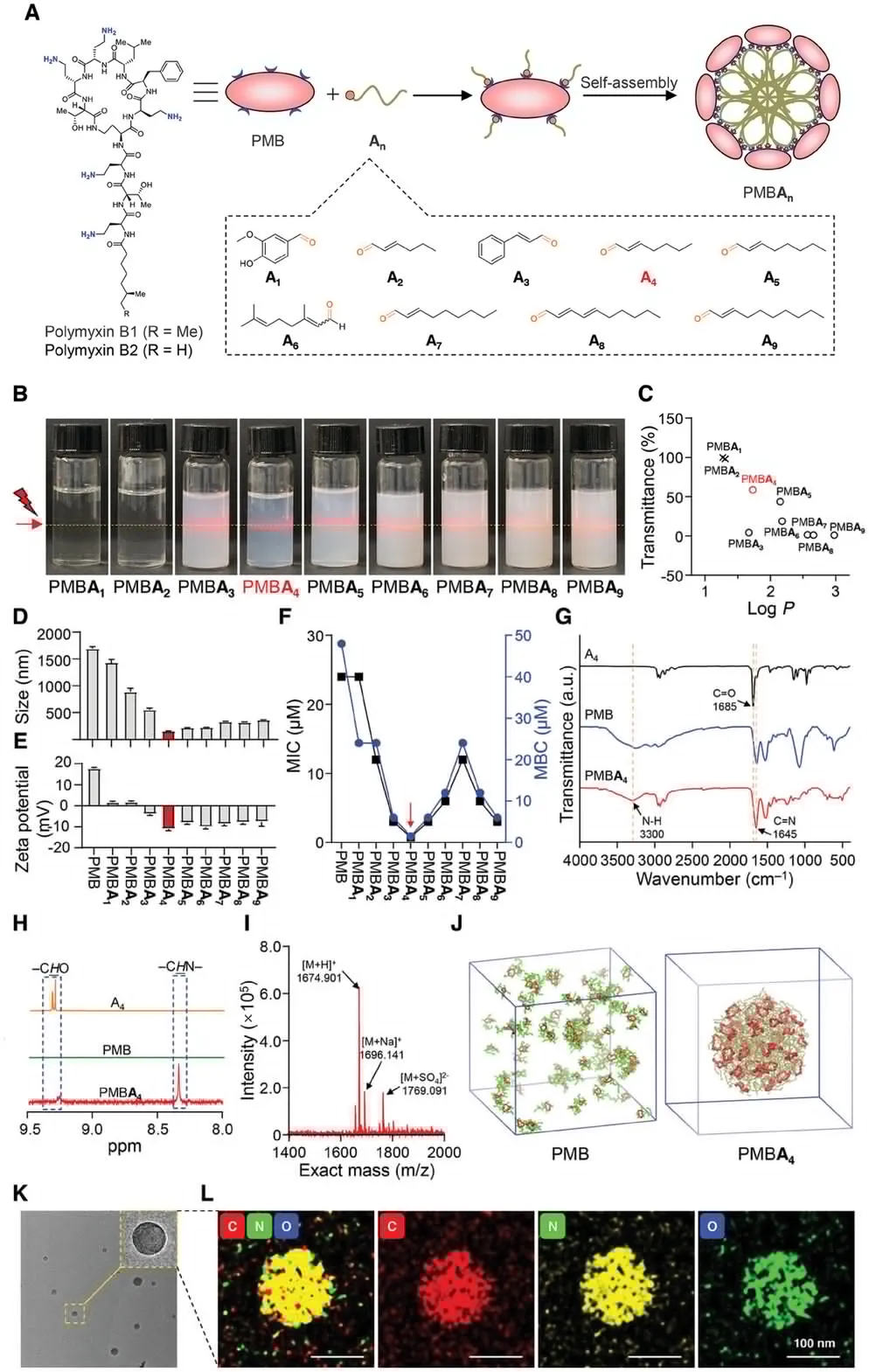
图1 RISA的构建及表征示意图(摘自Advanced Materials )
近期,相关学者基于动态共价键开发了新的药物负载策略。动态共价键在材料科学领域具有独特的优势,能够实现共价键的可逆形成和解离,实现自我修复、调控或重塑,具有高度的适应性和对环境变化的响应能力。此外,动态共价键能够精确控制复杂分子的结构特征,从而开发出具有定制性能的新型功能材料。通过采用动态共价键策略,作者成功地创建了包含多粘菌素、2-甲酰基苯硼酸和多酚的复杂纳米网络,有效地逆转了细菌耐药性并缓解炎症。然而,从临床转化的角度来看,这些纳米网络过于复杂。
为应对上述挑战,该研究报道了多粘菌素和天然醛类在水溶液中的反应诱导自组装(RISA),具有如下优点:(1)暂时屏蔽正电荷:可以暂时掩蔽多粘菌素的正电荷,防止其与带负电荷的哺乳动物细胞相互作用和潜在的细胞毒性;(2)生物膜的渗透和积累:纳米级特性使其能够渗透和积累在细菌生物膜中,增强多粘菌素的杀菌功效;(3)协同杀菌功效:存在于两亲性动物中的天然醛类可提供PMB的替代杀菌机制,逆转耐药性,预防耐药性的出现。除了上述优点外,该研究制备的动态共价两亲分子及其组装体极易合成,使其具备减轻与多粘菌素相关的细胞毒性和逆转耐药性的临床转化潜力。
参考消息:https://onlinelibrary.wiley.com/doi/full/10.1002/adma.202406156?saml_referrer
