严重发热伴血小板减少综合征病毒(SFTSV)的非结构蛋白(NSs)是重要的病毒毒力因子,通过将多种抗病毒蛋白质隔离到包涵体中,从而逃避抗病毒的先天免疫反应。然而,NSs限制宿主先天免疫的机制仍然很大程度上未被揭示。
2024年5月18日,武汉大学于学杰和周传敏共同通讯在Autophagy 在线发表题为“Bunyavirus SFTSV NSs utilizes autophagy to escape the antiviral innate immune response”的研究论文。该研究发现NSs通过与BECN1的CCD结构域相互作用,诱导完全的巨自噬,从而促进了依赖BECN1的自噬起始复合体的形成。重要的是,数据表明,NSs将TBK1等抗病毒蛋白质隔离到自噬小泡中,从而促进了TBK1及其他抗病毒蛋白质的降解。
此外,NSs的8A突变体减少了BECN1依赖的自噬流和抗病毒免疫蛋白质的降解。总之,结果表明,SFTSV的NSs通过将抗病毒蛋白质隔离到自噬小泡中进行降解,以逃避抗病毒免疫反应。
严重发热伴血小板减少综合征病毒(SFTSV)是一种经蜱传播的负链单链RNA/ssRNA病毒,引起了一种名为SFTS的严重新发出血热,死亡率高达30% 。自2010年以来,SFTS病例已在日本、韩国、巴基斯坦、越南、泰国和缅甸等地报告。SFTS的主要临床表现包括高热、血小板减少、白细胞减少,甚至多器官功能衰竭。SFTSV主要通过蜱咬传播,偶尔也通过接触患者体液而从人传人。2015年,世界卫生组织将SFTSV列入了可能引发国际公共卫生紧急事件的优先病原体名单。
SFTSV是一种三段RNA基因组的负链单链RNA/ssRNA病毒,包括大/L、中/M和小/S三个分段。大段编码RNA依赖性RNA聚合酶/RdRp,介导SFTSV病毒基因组的转录和复制。中段编码糖蛋白Gn和Gc,介导病毒的装配和进入细胞。小段编码核蛋白/NP介导SFTSV核糖核蛋白/RNP复合物的形成以及非结构蛋白(NSs)作为重要的毒力因子来逃避宿主抗病毒免疫反应。
先天免疫反应是对侵入病原体的第一道防线。宿主细胞利用模式识别受体/PRR,如RIGI(RNA传感器RIG-I)类受体/RLRs和toll样受体/TLRs,识别病毒感染,然后触发下游抗病毒干扰素(IFNs)信号传导,这对于保护宿主免受微生物感染至关重要。SFTSV已经发展了一些机制来规避宿主的防御,目前关于SFTSV逃逸宿主先天免疫反应的研究主要集中在SFTSV NSs抑制I型IFN产生。先前的研究表明,SFTSV NSs诱导了形成细胞质结构,称为包含体(IBs)。已证明NSs与抗病毒蛋白质如TBK1(TANK结合激酶1)、RIGI、IKBKE/IKKε(核因子kappa B抑制蛋白激酶亚基ε)、IRF3(干扰素调节因子3)和TRIM25(三部分结构域含25)等相互作用,并将它们隔离到IBs中,这被认为是抑制抗病毒先天免疫的。然而,NSs抑制抗病毒先天免疫的确切机制尚不清楚。
自噬是一种基本的细胞内降解过程,始于将细胞质蛋白和损坏的细胞器封入噬体中,噬体包裹吞噬的物质,形成自噬体,然后与溶酶体融合形成自噬溶酶体,以降解和回收被封闭的底物。BECN1已被认为是核心自噬调节蛋白,在自噬体形成步骤中起作用,并在定位于吞噬物蛋白到吞噬体组装位点中起关键作用。BECN1与几种辅因子(如ATG14、UVRAG和RUBCN)相互作用,以招募类III磷脂酰肌醇3-激酶PI3KC3/VPS34,并促进BECN1-PI3KC3复合体的形成,这对自噬和其他膜运输过程至关重要。
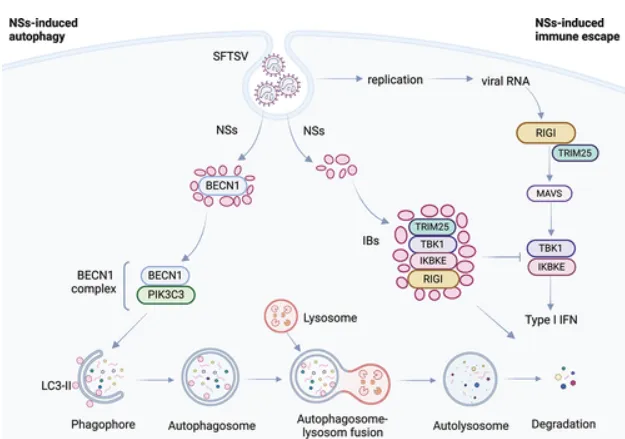
模式机理图(图片源自Autophagy )
自噬是一种保守的细胞防御机制,可以降解侵入的病毒颗粒,控制病毒复制并激活免疫应答。然而,许多病毒已经发展了各种策略来破坏和/或操纵自噬途径。到目前为止,关于SFTSV和自噬之间的关系的研究表明,SFTSV利用自噬来促进病毒的装配和释放。最近的研究还证明了SFTSV NSs在自噬中的作用。尽管SFTSV已被证明通过多条途径诱导自噬,但目前尚不清楚NSs是否可以通过自噬介导免疫逃避。在本研究中,作者旨在探索NSs诱导的自噬与免疫逃避之间的潜在联系。
原文链接:https://doi.org/10.1080/15548627.2024.2347103
