吞噬细胞清除凋亡细胞,这一过程被定义为胞葬作用(efferocytosis),对于维持组织稳态至关重要。每天机体会有数千亿个细胞会凋亡,并通过胞葬作用被清除,从而避免诱导炎症。吞噬细胞包括专职吞噬细胞(巨噬细胞)和非专职吞噬细胞(上皮细胞、成纤维细胞、内皮细胞等)。凋亡细胞也会在组织损伤、感染、神经退行性疾病和自免疾病等条件下局部积聚。在这些情况下,未清除的凋亡细胞会继发性坏死,加剧炎症。因此有缺陷的胞葬作用被认为是多种疾病的促成因素。在识别和去除凋亡细胞的过程中,磷脂酰丝氨酸(phosphatidylserine,PtdSer)的暴露起到核心作用。细胞凋亡后,PtdSer从质膜内层易位至外层。吞噬细胞上的受体与PtdSer结合。在直接识别PtdSer的受体中,TIM4直接结合PtdSer。BAL1是另一种可以直接与PtdSer结合的受体,它可以与胞质蛋白ELMO相互作用。ELMO与Dock180结合形成复合物,其作为小GTPase 蛋白Rac1的鸟嘌呤交换因子,促进胞葬作用中的细胞骨架重排。目前是否能够通过调控这些分子途径而改善胞葬作用,从而抑制疾病期间炎症发生,减少组织损伤还未知。
2022年12月22日,来自Virginia大学的 Kodi S. Ravichandran 团队在Cell 上发表题为Chimeric efferocytic receptors improve apoptotic cell clearance and alleviate inflammation 的文章。作者开发了新型嵌合受体,可以有效促进细胞的胞葬作用,清除凋亡细胞,降低炎症水平。
已经有研究在特定细胞中表达或者敲除胞葬相关受体,可以达到调控胞葬作用的效果。但是受体过表达发挥作用仍然需要募集细胞质信号中间体,这有可能限制调控效果。而且有些细胞类型也可能不表达下游信号中间体。为了克服这些困难,作者首先尝试将胞葬受体直接融合到信号中间体中。作者选择了ELMO1的C端包含195个氨基酸的结构域。这个结构域可以直接结合Dock180,从而有效模拟Rac激活和肌动蛋白重排,而且ELMO和Dock基本在所有细胞类型中表达。作者将ELMO1(aa 532-727)的C端结构域融合到胞葬受体BAI1,BAI1直接结合PtdSer,促进胞葬作用。作者把这种嵌合受体称为 “BELMO“。作者确认了BELMO表达在细胞表面后,开始对细胞的胞葬作用进行检测。发现过表达BELMO可以使细胞的胞葬作用增加5倍。作者又用延时成像以及流式验证了这一发现。作者还发现BELMO+细胞可以对吞入的凋亡细胞进行有效的酸化处理,这都表明BELMO可以有效增加细胞胞葬作用。
接下来为了验证体内效果,作者制作了转基因斑马鱼,将BELMO特异性表达在胶质细胞中。作者用局部激光脊髓损伤模型进行分析,对受伤部位每12分钟成像一次,观察持续10小时。对比发现BELMO阳性的胶质细胞胞葬作用更强,碎片清除速度更快。为了在哺乳动物中也验证BELMO的效果,作者制作了转基因小鼠,将BELMO特异性表达在单核/巨噬细胞中。用转基因小鼠的腹腔巨噬细胞检测发现,BELMO可以显著增加胞葬作用,并且还能促进细胞的抗炎作用。
作者用三种组织损伤模型对BELMO的促胞葬作用进行了进一步分析。作者分别用肠上皮细胞、肝脏细胞、肾脏小管上皮细胞特异性表达BELMO的小鼠进行了炎性肠病、肝脏毒性、肾脏毒性疾病模型分析。分析发现BELMO对疾病小鼠具有保护作用,但是这种保护作用只存在于局部组织,而不是整个机体。机制方面,作者发现多个与细胞蛋白质稳态相关的基因是细胞胞葬作用的限速因子。而细胞表达BELMO通过促进相关基因表达,改善蛋白质稳态,减少细胞毒性,从而获得更高水平的胞葬作用。
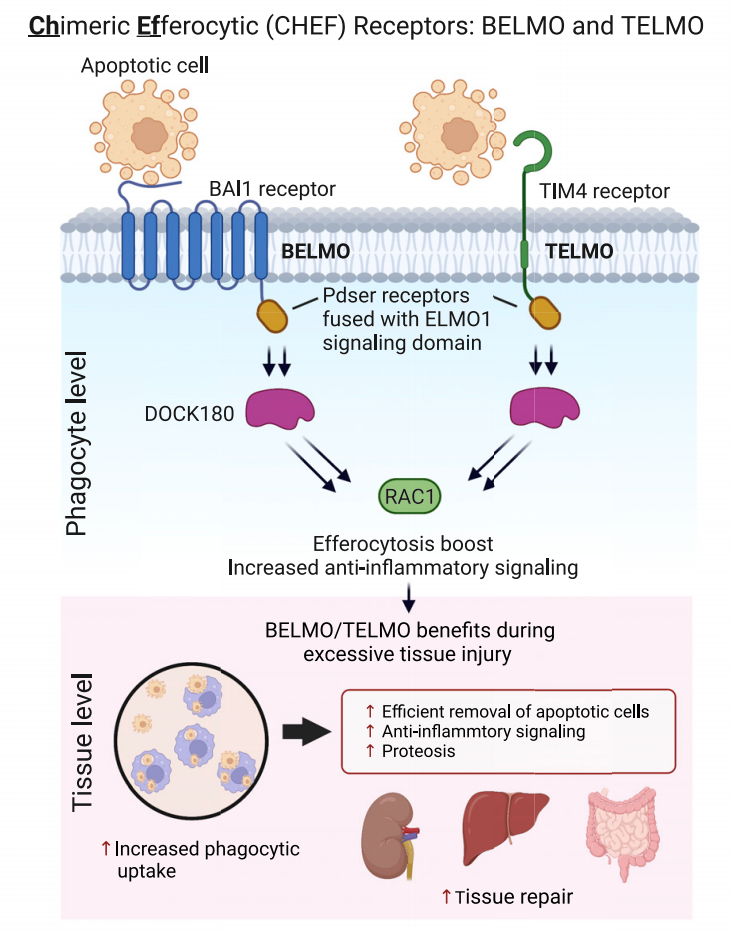
本研究开发了一种嵌合细胞受体BELMO,突破先前胞葬作用调控的局限,可以更为高效地促进胞葬作用,清除凋亡细胞,降低炎症水平,在多种疾病模型具有局部保护作用。
原文链接:
https://doi.org/10.1016/j.cell.2022.11.029
